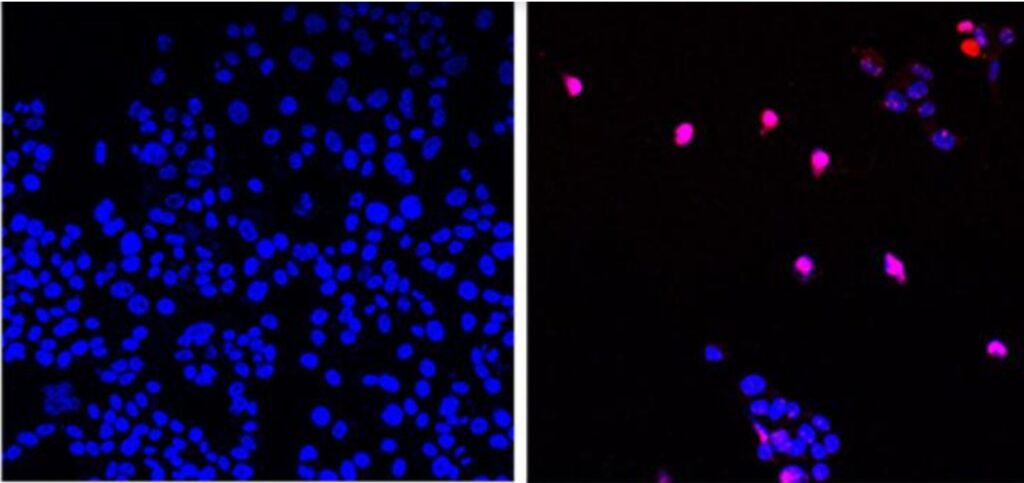
Hier sehen wir unbehandelte Krebszellen (links) und mit AOH1996 behandelte Krebszellen (rechts), die einen programmierten Zelltod erleiden (violett). (Bildnachweis: Stadt der Hoffnung)
Krebserkrankungen zählen aktuell immer noch zu den häufigsten Todesursachen.
Doch die Behandlungsmöglichkeiten verbessern sich für viele Tumore schon seit längerem.
Nun hat das größte Krebsforschungszentrum der USA, City of Hope, eine neue Studie veröffentlicht, die vielversprechend klingt. Die Studienergebnisse zu einer Anti-Krebs-Pille soll gegen 70 Krebsarten wirken.
Ein Durchbruch in der Krebsforschung?
Es geht bei der Anti-Krebs-Pille um das Medikament AOH1996, das auf ein bestimmtes Protein in der Krebszelle abzielt, das PCNA, Proliferating Cell Nuclear Antigen. Das PCNA spielt eine wesentliche Rolle bei der Vermehrung und Reparatur von Tumor-Zellen. Das Medikament greift PCNA an und hemmt so das Wachstum und auch die Ausbreitung von Krebszellen. Das Gute daran: Das Medikament ist für gesunde Zellen nicht toxisch (giftig).
Bei jeglicher Krebstherapie kommt es darauf an, nur die Krebszellen zu erwischen und die gesunden Zellen in Ruhe zu lassen. Deshalb konzentrieren sich die meisten zielgerichteten Therapien bislang auf einen einzigen Weg. Das aber ermöglich es heimtückischem Krebs, zu mutieren (spontane Änderung im Erbbild) und schließlich resistent (widerstandsfähig) zu werden. Das neue Medikament führte nun dazu, dass Krebszellen abgetötet wurden – ohne dass der Fortpflanzungszyklus gesunder Stammzellen unterbrochen wurde. Dabei hat es sich in der präklinischen Forschung zur Behandlung von Zellen z.B. aus Brust-, Prostata-, Gehirn-, Eierstock-, Haut-, Gebärmutterhals- und Lungenkrebs als wirksam erwiesen.
AOH1996 kann das Tumorwachstum als Monotherapie wie auch in Kombinationsbehandlung in Zell- und Tiermodellen unterdrücken. Außerdem zeigte sich, dass AOH1996 gleichzeitig Krebszellen anfälliger für andere chemische Wirkstoffe machte – wie etwa das Chemotherapeutikum Cisplatin.
Da sich die Versuchsreihe mit dem Medikament nicht nur aufs Reagenzglas, sondern auch bei Tierzellen Erfolge zeigen, stimmt positiv, so dass AOH1996 bereits im vergangenen Jahr das erste Mal einer Krebspatientin verabreicht wurde.
In der nächsten Phase muss das Medikament weiter am Menschen getestet werden. Erst dann zeigt sich, ob sich die Erfolge, die das Medikament in den bisherigen Versuchen gezeigt hat, wiederholen lassen. Bis ein Medikament zugelassen werden kann, müssen alle drei klinischen Studienphasen durchlaufen werden. Das nimmt in der Regel mehr als zehn Jahre in Anspruch.
Phasen der Medikamentenentwicklung
In der Pharmaforschung wird in Pharmaunternehmen und Universitäten gezielt nach neuen Wirkstoffen, neuen Wirkstoffkombinationen, neuen galenischen Formen, neuen Anwendungsgebieten für bestehende Arzneimittel und die Entwicklung neuer Arzneimittel gesucht. Erweist sich ein Stoff oder eine Wirkkombination als aussichtsreich, folgen die nächsten Entwicklungsphasen:
Präklinische Phase
Die neu entwickelten Wirkstoffe werden zunächst in Zellkulturen (in vitro, im Reagenzglas) und Tiermodellen (in vivo, im Lebendigen, also zuerst im Tierversuch, später an Menschen) auf deren Wirksamkeit und Sicherheit getestet.
Klinische Phase
Phase I – Studie mit wenigen Gesunden
Waren die präklinischen Tests positiv, wird der Wirkstoff an erwachsenen, gesunden Freiwilligen erprobt. Dabei werden vor allem die Aufnahme und der Abbau des Wirkstoffs sowie die optimale Dosis untersucht.
Phase II – Studien mit wenigen Erkrankten
Auf Basis der ermittelten Dosis aus der Phase-I-Studie wird der Wirkstoff an freiwilligen Erkrankten erprobt. Dabei stehen Wirksamkeit (im Vergleich zu Placebo = Scheinmedikament und herkömmlichen Medikamenten), Verträglichkeit und Dosierung im Fokus.
Phase III – Studien mit vielen Erkrankten
Ärztinnen und Ärzte in vielen Ländern erproben die Substanz an einer sehr großen Gruppe von freiwilligen Erkrankten. Dadurch werden weniger häufige Nebenwirkungen identifiziert.
Zulassung
Begutachtung der Zulassungsbehörde: Fachleute prüfen nochmals die Ergebnisse aller Studien. Fällt die Prüfung positiv aus, kann das Medikament zugelassen und kann fortan Patienten verordnet werden.
Phase IV – Studien nach der Zulassung
Das Medikament wird in weiteren Studien erprobt, zum Beispiel um zu sehen, wie es mit anderen Mitteln zusammenwirkt oder ob es für die Behandlung weiterer Krankheiten in Betracht kommt.
(Quelle: Fraunhofer CIMD) aus Focus.de, Donnerstag, 03.08.2023, 08:42